11月3日,中国科学技术大学化学与材料科学学院、中科院软物质化学重点实验室刘世勇教授课题组在国际学术期刊《自然-化学》(Nature Chemistry) 上发表了题为 “Digital micelles of encoded polymeric amphiphiles for direct sequence reading and ex vivo label-free quantification” 的研究论文。该工作报道了精准编码两亲性高分子的合成和在质谱测序、数码胶束构建以及复杂生物体系中无标记定量中的研究。
定量研究聚合物纳米粒子的生物分布对于评估纳米药物的诊疗效果及体内命运至关重要。常见的荧光和同位素标记技术主要依赖于化学修饰,而化学修饰后可能改变聚合物纳米粒子的理化性质进而影响其生物分布。同时,传统聚合物由于分子量的宽分布、链长不均一、序列不明确等固有特性导致无标记定量聚合物极具挑战性,这些固有的局限性也直接影响聚合物纳米药物的临床转化。因此,发展聚合物纳米粒子的精确量化策略对于进一步推动纳米医学的设计和转化具有重要意义。
经过充分的前期调研,研究人员设想如果聚合物能满足以下要求,则可用质谱实现聚合物的精准定量:1) 聚合物结构精确,具有适当的单一分子量,以避免丰富生物大分子的干扰;2) 易于识别,可实现聚合物序列直读和无标记定量;3)可有效离子化,在复杂的生物体系中具有高质谱检测灵敏度。
为了实现这一目标,研究人员首先设计并以模块化合成策略创制了一系列由光敏感触发基元、N-芳基氨基甲酸酯重复单元和树枝状PEG (PEG dendron) 三部分组成的精准编码两亲性高分子。MALDI-TOF一级谱的单峰证明了该精准两亲性高分子具有单一分子量。进一步的串联质谱表明,PEG dendron与碱金属离子(如钠离子) 的超分子识别和主链中苄氧键选择性断裂的协同作用实现了聚合物序列的直读 (图1)。
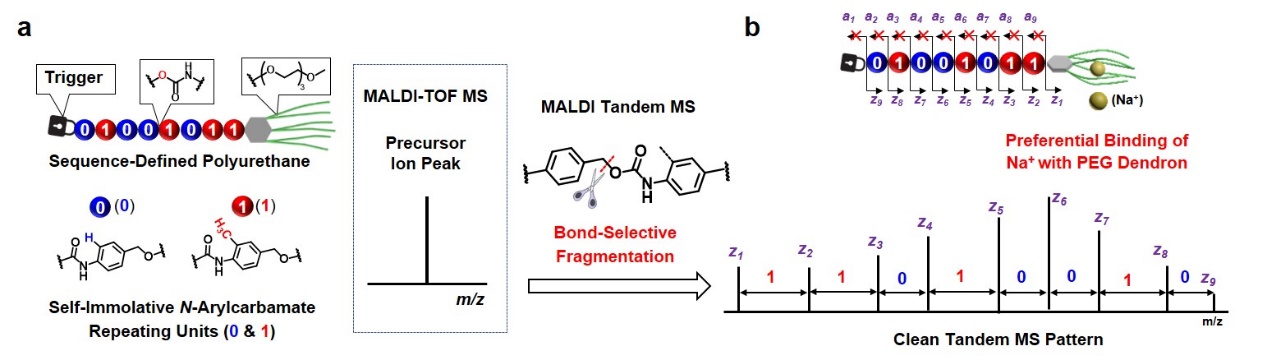
图 1. 精准编码两亲性聚合物的序列直读。
此外,研究人员还发现这些新型精准编码两亲性聚合物可以自组装成不同形貌的数码胶束,其组装形貌受到聚合物主链序列的严格控制,这为探索纳米粒子在体内的命运提供了丰富的软物质纳米载体模型 (图2)。
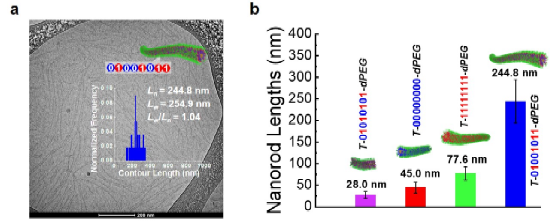
图2. 不同序列的精准编码两亲性聚合物自组装成长度可控的数码胶束。
基于精准编码两亲性聚合物的合成、测序,以及数码胶束的成功构建,研究人员进一步探究了数码胶束在生物体系中精准定量的可能性。首先研究人员通过对照实验证明了聚合物合理的分子量设计可规避生物(大)分子对MALDI质谱测试的干扰。随后将四种典型的数码胶束 (一种球状胶束和三个不同长度的棒状胶束)等量混合,通过尾静脉注入大鼠体内,在不同的时间点取出主要器官,并对器官进行研磨、冻干和萃取操作。基于此,研究人员以无标记定量的方式系统研究了不同数码胶束在大鼠器官中的生物分布。此外,由于PEG dendron对精准编码两亲性聚合物MALDI检测灵敏的增强作用,研究人员进一步对组织切片 (如脾脏切片) 进行MALDI成像,并揭示了数码胶束在器官中的空间分布 (图3)。
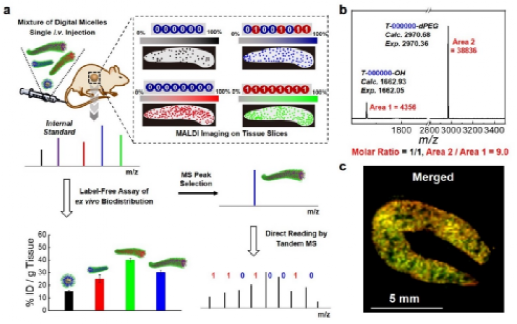
图3. 在器官和组织切片水平上对数码胶束进行识别和无标记定量。
本工作为解决聚合物纳米粒子的生物分布定量问题提供了全新思路,且PEG dendron增强的MALDI定量和解码策略可以进一步用于多肽/蛋白质/DNA和其他天然/合成分子的测序及定量研究。当前,该课题组正在基于这一进展开展三方面的深入研究:1) 基于数码胶束无标记定量技术的蛋白质组学与蛋白冠主动精准调控;2) 基于数码油墨的无法反向破解的加密打印和信息安全存储;3)基于该类单链选键化学和精准高分子材料化学创制单一组分极紫外光刻胶,这一设想已在中国科大微纳研究与制造中心的全力配合下获原理性验证。
中国科大化学与材料科学学院博士生石强强为该论文第一作者,刘世勇教授为该论文通讯作者。中国科大理化科学实验中心质谱实验室为本工作的大分子质谱分析与质谱成像提供了全方位支持;冷冻电镜测试由西安交通大学张彦峰教授和童慧敏博士完成;上海同步辐射光源BL19U2生物小角散射线站提供了测试机时,李娜研究员为SAXS数据采集和分析提供了专业指导;深圳大学李霄鹏教授和苏州大学张正彪教授在电喷雾质谱/大分子质谱分析、数据讨论和论文撰写方面提供了重要指导。本工作得到了国家自然科学基金重大项目、重点项目、创新研究群体项目、区域创新基金项目,以及科技部国家重点研发计划“变革性技术关键科学问题”重点专项项目支持。
原文连接:https://www.nature.com/articles/s41557-022-01076-y
